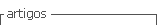Introdução
A trombocitemia essencial (TE) é uma neoplasia mieloproliferativa crónica caracterizada pela proliferação clonal de células mieloides que origina produção plaquetária excessiva.1 Trata-se de uma condição pouco comum, tendo uma incidência estimada de 0,38 a 1,7 novos casos por 100.000 habitantes por ano na União Europeia. 2 A incidência aumenta com a idade e a idade média ao diagnóstico ronda os 60 anos. No entanto, em cerca de 20% dos casos os indivíduos têm menos de 40 anos. 1-2
Alguns indivíduos são assintomáticos. 1 Contudo, a TE pode manifestar-se através de sintomas como cefaleias, síncope, vertigem, dor torácica, parestesias acrais, livedo reticular, eritromelalgia e distúrbios visuais transitórios. 1 Encontram-se descritos sintomas mais raros e inespecíficos, como fadiga, enfartamento precoce e desconforto abdominal. 3 Os eventos hemorrágicos e tromboembólicos são os grandes riscos desta patologia. 1 Na maioria dos casos verifica-se a presença de mutações nos genes JAK2, MPL ou CALR. 4 Embora não exista nenhum marcador 100% específico, mais de metade dos casos têm a mutação JAK2 V617F presente. 5-6 De referir que a presença de uma neoplasia mieloproliferativa com mutação JAK2 V617F aumenta em 27,7 vezes o risco de desenvolver uma trombose da veia porta. 4
A partilha do presente caso clínico tem como objetivo alertar para uma patologia que, embora rara, pode passar despercebida e causar eventos potencialmente graves. A importância de um estudo mais atento, descartando outras causas de trombocitemia, revela-se importante para a prática clínica de um médico de família, bem como a referenciação atempada. 7
Descrição do caso
Utente do sexo feminino, 43 anos, caucasiana, solteira, habilitada com o 12.º ano de escolaridade, escriturária, natural do Funchal e residente no Porto, pertencendo a uma família unitária.
Antecedentes pessoais de hepatite B crónica diagnosticada em 2013, mantendo seguimento em consulta de Infeciologia. Negava antecedentes cirúrgicos ou outras doenças crónicas. Negava medicação habitual, incluindo método contracetivo hormonal. Não se encontrava grávida nem mantinha atividade sexual. Negava hábitos tabágicos, alcoólicos ou abuso de substâncias psicotrópicas. O plano nacional de vacinação encontrava-se atualizado.
Recorreu a consulta aberta na unidade de saúde, a 20/agosto/2020, referindo queixas de enfartamento precoce, dispepsia e epigastralgia com três dias de evolução. Negava alterações gastrointestinais, nomeadamente náuseas, vómitos ou alterações das características habituais das fezes. Ao exame físico apresentava-se com bom estado geral e anictérica. Abdómen sem evidência de circulação colateral, ruídos hidroaéreos presentes e sem alterações, timpânico na zona da fossa ilíaca esquerda, mole, depressível, indolor e sem massas ou organomegalias. No contexto do seguimento hospitalar supracitado, a utente realizava regularmente estudo analítico. Os parâmetros avaliados encontravam-se dentro dos valores de referência, exceto o valor absoluto de plaquetas (Tabela 1). Desde há três anos que a utente apresentava sistematicamente valores a rondar as 500.000 plaquetas por mm3. A utente tinha uma endoscopia digestiva alta realizada no início do mesmo ano com resultado normal. No sentido de estudar esta sintomatologia foi solicitada ecografia abdominal.
Em 15/setembro/2020 é reavaliada na unidade de saúde com o resultado da ecografia abdominal que descrevia o seguinte: “Observa-se trombose parcial da veia porta e praticamente completa do seu ramo esquerdo, que tem calibre já ligeiramente reduzido. É difícil avaliar se este trombo apresenta vascularização no estudo doppler. O fígado revela morfologia globosa e dimensões ligeiramente aumentadas, medindo 15,6 cm de eixo longitudinal na linha medio-clavicular. Apresenta textura parenquimatosa difusamente heterogénea, em particular no lobo esquerdo. Há vários quistos hepato-biliares dispersos peri e infracentimétricos. Baço de dimensões aumentadas de textura homogénea, medindo 15 cm de eixo longitudinal. Pequeno baço acessório adjacente ao hilo esplénico com 14 mm. Na vesícula biliar visualiza-se um pequeno pólipo parietal com 2 mm, posteriormente a reavaliar. Sem ascite.” A utente refere que, perante alteração da ecografia, optou por recorrer a médico particular, tendo sido medicada com enoxaparina 60 mg 12/12horas. Como tinha consulta agendada para infeciologia para o próprio dia optou-se por delegar a continuação do estudo para a consulta hospitalar.
Posteriormente verificou-se que, na consulta de infeciologia, foi feito um pedido de angiotomografia computorizada (angio-TC) abdominal superior e estudo pró-trombótico, incluindo pesquisa de mutação do fator V Leiden e de polimorfismo G20210A da protrombina, bem como doseamentos de proteína C e S, antitrombina, anticoagulante lúpico, anticorpo anticardiolipina, anti-β2-glicoproteína e homocisteína. Foi também realizado pedido de estudo genético com pesquisa de mutação JAK2 V617F. Por fim, a utente foi referenciada internamente para a consulta de hematologia clínica.
Em 06/outubro/2020 a utente foi reavaliada em consulta de infeciologia, em que o angio-TC abdominal superior apresentava o seguinte relatório, confirmando a presença de trombose ao nível do sistema venoso portal: “O fígado apresenta morfologia globosa e dimensões no limite superior da normalidade, com textura heterogénea incluindo múltiplos quistos simples dispersos por ambos os lobos, o maior dos quais à direita no segmento VII, medindo 24 mm. Não há lesões nodulares sólidas ou com captação suspeita do produto de contraste. Observa-se um aumento do calibre do tronco da veia porta que mede 16 mm, vendo-se a este nível um trombo no seu interior. Há também amputação do ramo esquerdo da porta por trombose crónica deste segmento. O ramo direito apresenta calibre conservado com esboço de diminutas imagens hipodensas/defeitos de preenchimento no seu interior, sobretudo no ramo anterior, indiciando incipiente trombose a este nível. Baço com dimensões aumentadas medindo 13,7 cm maior diâmetro longitudinal com densidade homogénea sem evidência de lesões focais. Observam-se colaterais porto-sistémicos incluindo incipientes varizes gástricas. Restante exame dentro dos parâmetros da normalidade”. À data da consulta ainda não havia resultados do estudo genético e o restante estudo apresentava-se sem alterações. Perante a confirmação da suspeita de trombose da veia porta e resultados do estudo analítico foi iniciada varfarina 5 mg 1x/dia coadjuvante à enoxaparina 60 mg 12/12 horas e a utente foi orientada para a consulta de imuno-hemoterapia.
Em 09/dezembro/2020 a utente foi avaliada em consulta de hematologia. No estudo genético foi confirmada a existência da mutação V617F no gene JAK2, pelo que foi assumido o diagnóstico de TE. Iniciou tratamento de citorredução com hidroxiureia 500 mg em dias alternados.
Foi mantido o seguimento nas consultas hospitalares durante os meses seguintes, com estudo analítico de controlo com valores de plaquetas ainda acima do valor recomendado (520.000 plaquetas/mm3 em 23/maio/2021).
Em agosto/2021 foi repetido o angio-TC abdominal, que evidenciou nova trombose, com o seguinte resultado: “O fígado tem dimensões preservadas, com contornos ligeiramente lobulados e ligeira hipertrofia do lobo esquerdo. Identificam-se múltiplos quistos simples (…) mas sensivelmente sobreponíveis. (…) Observa-se trombo na veia porta de aspeto alongado e cuja extensão é sobreponível ao exame de confronto. Trombose da veia esplénica com extensa circulação colateral no abdómen superior, destacando-se presença de varizes gástricas. A veia mesentérica superior encontra-se patente. O tronco celíaco e artéria mesentérica superior encontram-se patentes. Os rins têm normal morfologia e dimensões (…). Não se observa líquido livre ou adenomegalias nos planos abdominais abrangidos”.
Dado o diagnóstico de nova trombose sob citorredução com hidroxiureia, em novembro/2021 foi feita mudança para interferão peguilado (IFN-Peg) 45 microgramas 1xsemana via subcutânea. A utente manteve-se com este tratamento até setembro/2022, apesar da baixa tolerância, altura em que voltou a fazer hidroxiureia em dias alternados.
Comentário
A trombose venosa é um dos riscos associados à TE. O caso apresentado pelos autores reveste-se de relevância uma vez que a utente em causa apresentava um valor absoluto de plaquetas ligeiramente superior ao limite superior do intervalo de referência. Além disso, apesar de a utente se apresentar sintomática, o sintoma cardinal não era dos mais comummente descritos. As queixas abdominais poderiam facilmente ser associadas a uma causa gastrointestinal. Contudo, a deteção de um valor anormal de plaquetas precipitou a investigação, que levou à deteção da trombose da veia porta, que poderia justificar as queixas abdominais, e posteriormente ao diagnóstico de TE. 8
Mediante a presença de uma trombocitemia, mesmo que ligeira, revela-se importante o estudo e diagnóstico diferencial com trombofilias adquiridas ou hereditárias e outras neoplasias da linhagem mieloide, de forma a orientar o tratamento. 9 Um estudo inicial, feito nos cuidados de saúde primários (CSP), passa por um hemograma completo com avaliação do esfregaço de sangue periférico, perfil hepático, função renal, ionograma, LDH, ácido úrico e cinética do ferro. 10 Posto isto, é indispensável a referenciação a consulta hospitalar de hematologia na suspeita de trombofilia hereditária e após despiste de trombofilia adquirida, visto que a confirmação diagnóstica implica meios auxiliares de diagnóstico não existentes ao nível dos CSP (e.g., mielograma e estudo genético). 9-10 No caso de utentes com hepatite B crónica, a trombose da veia porta pode ser surgir como consequência de um carcinoma hepatocelular, pelo que é imperativa a sua exclusão. 11 Nesta utente, essa possibilidade foi excluída tanto pela ecografia como pelo angio-TC abdominal. Não foi encontrada evidência de que a existência desta infeção crónica hepática viral afete o prognóstico da TE. 12
Note-se que a suspeita da trombocitemia essencial ocorre ao nível dos CSP; no entanto, é importante a referenciação para os cuidados de saúde secundários, não só para a confirmação diagnóstica como também para o tratamento, visto apenas estar disponível ao nível hospitalar.
A anticoagulação é a base do tratamento da trombose da veia porta. O tratamento habitual inicia-se com heparina não fracionada ou, mais comummente, com heparina de baixo peso molecular (tipicamente enoxaparina na dose de 1 mg/kg 12 h/12 h), seguindo-se um período intermédio de sobreposição com varfarina, ficando por fim esta última em monoterapia a longo prazo para um INR entre 2 e 3. 4 Os anticoagulantes orais diretos têm vindo a ganhar destaque pela facilidade de administração e ausência de necessidade de monitorização. 4
O tratamento da TE é orientado mediante a estratificação do risco de cada utente. 1,10,13 Consideram-se de risco médio-alto utentes em qualquer idade com TE e que apresentam evento tromboembólico documentado. 1,13 Nestes utentes está preconizado realizar tratamento citorredutor com hidroxiureia, com ajuste de dose para manutenção de contagem de plaquetas entre 100.000 e 400.000/microL e evitando neutropenia e anemia, acompanhado de anticoagulação por seis meses. 1,9
A partilha do presente caso clínico pretende alertar os médicos de família para a importância de valorizar a sintomatologia e realizar um estudo atento, valorizando pequenas variações sustentadas fora dos intervalos da normalidade e, na necessidade de aprofundá-lo, fazer uma referenciação correta e atempada de modo a evitar desfechos graves.
Contributo dos autores
Conceptualização, TCF, PFT, LFS, MB, NMP, FM, GF e MM; metodologia, TCF, PFT, LFS, MB, NMP, FM, GF e MM; investigação, TCF, PFT, LFS, MB, NMP, FM, GF e MM; recursos, TCF, PFT, LFS, MB, NMP, FM, GF e MM; redação do draft original, TCF, PFT, LFS, MB, NMP, FM, GF e MM; revisão, edição e validação do texto final, TCF, PFT, LFS, MB, NMP, FM, GF e MM; visualização, TCF, PFT, LFS, MB, NMP, FM, GF e MM; supervisão, TCF, PFT, LFS, MB, NMP, FM, GF e MM; administração do projeto, TCF, PFT, LFS, MB, NMP, FM, GF e MM.